17 декабря 1991 года в Советском Союзе была проведена первая успешная трансплантация костного мозга (ТКМ) у ребенка. Пациентом стал мальчик с острым лимфобластным лейкозом. Процедуру провел профессор Борис Владимирович Афанасьев. Его первый пациент жив до сих пор, а за эти 30 лет были проведены тысячи трансплантаций. Профессор Зубаровская была рядом с Афанасьевым в тот исторический момент, сегодня она возглавляет отдел детской онкологии, гематологии и трансплантологии в петербургском НИИ детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой. «Хайтек» вместе с благотворительным фондом AdVita поговорил с Людмилой Степановной о том, как происходила подготовка к первой ТКМ, какие альтернативы пересадке костного мозга появились и как сегодня справляются с реакцией «трансплантат против хозяина».
«Его волновала не историчность события, а чтобы ребенок выздоровел»
— Как в нашей стране появилась процедура ТКМ и насколько первая трансплантация, проведенная профессором Борисом Владимировичем Афанасьевым, была уникальной?
— Эта методика появилась на Западе примерно с начала 50-х годов. В 60-е прошли первые успешные эксперименты на животных. Но изначально ТКМ создавалась для экстремальных ситуаций, прежде всего, связанных с развитием атомной энергетики. Трагические события в Японии послужили катализатором для разработок в этой области, чтобы защитить людей, занятых в ядерной отрасли или ставших жертвами взрывов атомных бомб в Хиросиме и Нагасаки, а спустя 40 лет — аварии на ЧАЭС.
В 1968 году была проведена первая успешная трансплантация костного мозга от другого человека ребенку с врожденным иммунодефицитом — в семье ребенка было 11 случаев подобного заболевания с летальным исходом. Процедуру выполнили американские врачи в Санкт-Петербурге, США. Кстати, этот пациент до сих пор жив. И именно его случай можно считать датой зарождения метода ТКМ. Вслед за этим стали появляться новые центры трансплантологии, главный из которых на тот период был в Сиэтле, США.
В СССР вообще не было такого направления, хотя советские гематологи осознавали всю необходимость внедрения метода ТКМ, поскольку без него невозможно было эффективно лечить пациентов.
Именно Бориса Владимировича тогда и отправили на стажировку в Сиэттл, где он пробыл около четырех месяцев. А по возвращении начал под эту технологию создавать отделение в Ленинграде. Но что значит создавать?! В то время не было ни специализированных клиник, ни тем более докторов, знакомых с ТКМ, не было медсестер, инфраструктуры, от которой крайне зависит эффективность лечения.

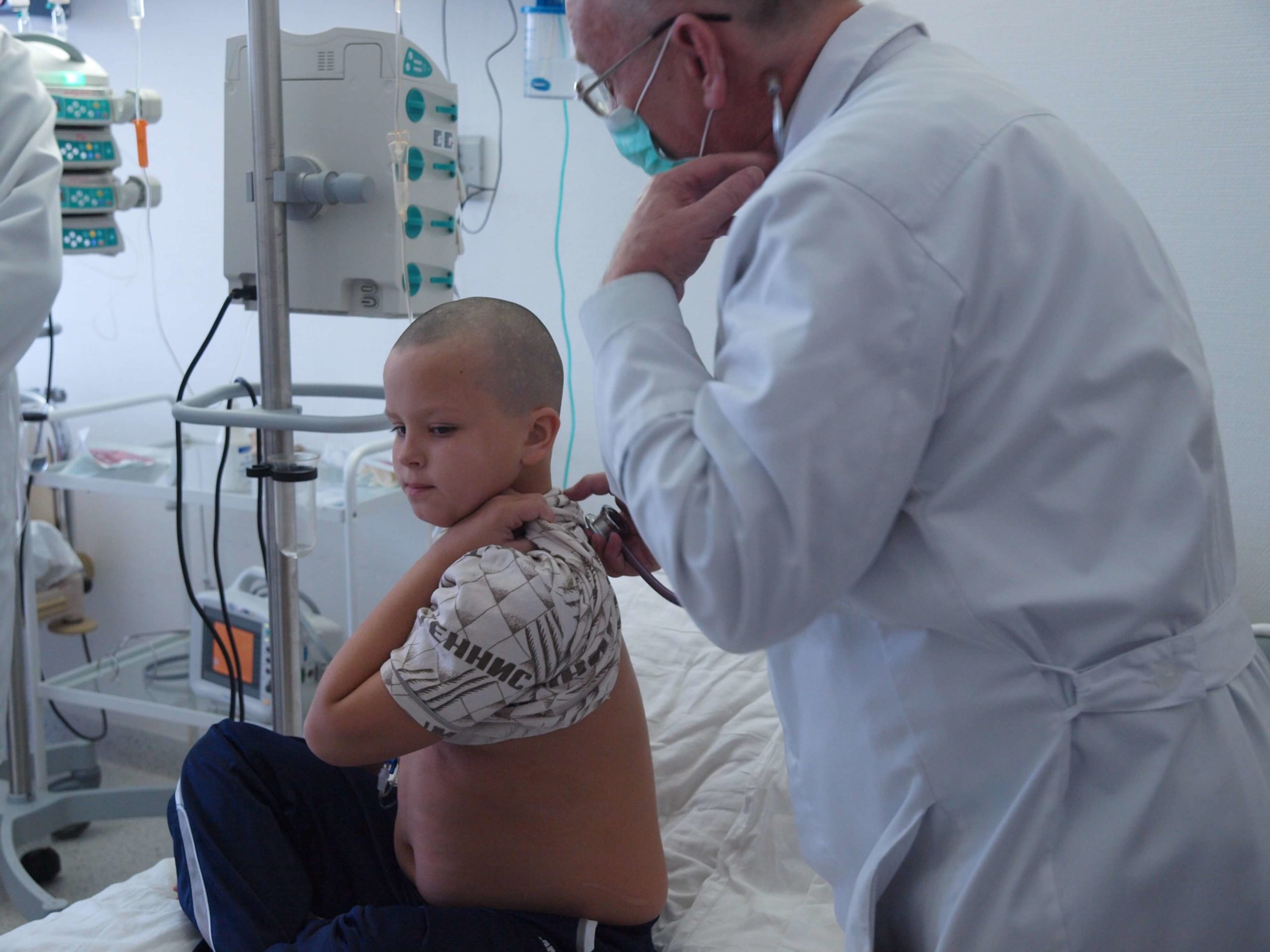
Фото предоставлено НИИ детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой
Пациенты появились в отделении в начале 90-х, тогда же и была проведена первая процедура ТКМ — к нам поступил мальчик с острым лимфобластным лейкозом. Ему требовалась трансплантация, поскольку мы уже исчерпали все возможные ресурсы химиотерапии. Его брат оказался совместимым донором, и в декабре 1991 года прошла первая в истории нашей страны пересадка костного мозга.
Острый лимфобластный лейкоз — злокачественное заболевание системы кроветворения, характеризующееся неконтролируемой пролиферацией незрелых лимфоидных клеток (лимфобластов). Острый лимфобластный лейкоз является самым распространённым злокачественным заболеванием в детском и юношеском возрасте.
— Вы были рядом с Афанасьевым в этот момент. Как себя чувствует человек, которому предстоит такая историческая процедура?
— На этот вопрос ответить невозможно. Борис Владимирович волновался за пациента, как все пройдет, чтобы не было осложнений. Это суперстрессовая ситуация для врача.
Борис Владимирович был человеком, который всегда глубоко погружался в проблему. Поэтому решения давались ему нелегко: та ответственность, которую он взял на себя, подразумевала очень большое напряжение. Хотя главным для профессора Афанасьева была не историчность события, а чтобы ребенок выздоровел.
Но тут стоит отметить, что, да, это была первая трансплантация, но за ней же последовали вторая, третья, и даже сейчас ТКМ — это эмоционально очень серьезная процедура.
Каждый год в клинике Института у детей выполняют до 190 трансплантаций всех видов — аутологичных, родственных и неродственных аллогенных от доноров с разной степенью совместимости. Всего в НИИ ДОГиТ им. Р. М. Горбачевой проводят порядка 400 ТКМ в год у детей и взрослых.
«Иногда мы радуемся, что выживаемость пациентов — 50%, а ведь без ТКМ могла быть 10%»
— А если сравнить: как изменилось соотношение смертность/выживаемость пациентов, которые прошли через ТКМ, спустя 30 лет после первой процедуры?
— Безусловно, есть диагнозы, где выживаемость была на уровне 15–20%, а сейчас она достигает 70–90%. Конечно, эффективность лечения зависит от конкретного диагноза и самих пациентов. Поэтому иногда мы радуемся, что у нас выживаемость пациентов находится на уровне 50%, а ведь могла быть и 10% — без ТКМ. Здесь очень сложно оперировать цифрами, потому что это люди, они страдают ужасными и разнообразными заболеваниями, и объединить их в одну статистику не представляется возможным — это будет попросту неправдой.

— Процедура поиска донора и сама трансплантация все равно остается достаточно дорогостоящей?
— Да, но здесь за последние годы произошли изменения. Конечно, процедура была очень дорогостоящей, когда мы пользовались только зарубежными регистрами. Сейчас в России работает свой регистр потенциальных доноров костного мозга. Кроме того, сейчас для детей развита трансплантация от родителей, что тоже снижает материальные затраты.
— Благотворительные фонды тоже оплачивают лечение?
— Да, благотворительность имеет огромное значение, поскольку многие этапы лечения стоят куда дороже, чем это заложено государством. Кроме того, сейчас много новых препаратов, которые еще не оплачиваются в той мере, в которой это необходимо. И значение благотворительности будет возрастать, причем такая ситуация во всем мире. Например, фонд AdVita, в создании которого мы принимали участие, занимается широким спектром задач: и донорами, и лекарственными препаратами, обследованием и проживанием пациентов — социально-бытовые моменты тоже важны во время лечения и часто приносят много проблем.
Стоимость поиска и активации доноров
- В крупнейшем немецком регистре им. Стефана Морша — 23 000 евро (дополнительно оплачивается доставка трансплантата в Россию — 371 200 рублей).
- Поиск в российском регистре в среднем обходится от 291 000 до 400 000 рублей (с учетом доставки трансплантата, если донор находится в другом городе).
В настоящее время в фонд AdVita обратились 15 человек, которым нужно помочь с оплатой поиска и активации донора костного мозга из российского регистра. Одному подопечному требуется оплата донора из Германии. Помочь можно по ссылке или просто нажмите на кнопку снизу:
ХОЧУ ПОМОЧЬ— Сегодня люди уезжают из России за рубеж, чтобы провести ТКМ? Насколько российские пациенты получают своевременное лечение по современным протоколам?
— Нет, сейчас почти не уезжают. В нулевых некоторые уезжали во многом по эмоциональным проблемам, пациенты или их семьи не доверяли нашей медицине. Сейчас это фактор практически нулевой, кроме того, на Западе все баснословно дорого, а у нас это оплачивается государством.
— А к нам приезжают из-за рубежа для проведения трансплантации?
— В основном из стран с постсоветского пространства — это Армения, Узбекистан. Раньше были пациенты из Казахстана, но там открыли свою клинику. Похожая история с Болгарией и Польшей — оттуда приезжали люди, пока в этих странах не было своих клиник и технологий.
— Какие сегодня существуют центры трансплантологии в России?
— У нас очень большая страна, и наличие региональных центров — крайне важная история. Но, безусловно, создание клиник требует множества условий: от специалистов и инфраструктуры до финансирования. Поэтому преимущественно это большие города. В Петербурге и Москве есть центры для взрослых и детей. В Екатеринбурге открыта детская клиника. В ближайшем будущем появятся центры в Челябинске и Красноярске, тоже детские, в следующем году — в Краснодаре.
- На сегодняшний день в российских регистрах имеются данные о более чем 158 000 потенциальных доноров. Для сравнения: 8,6 млн — в США, 8,1 млн — в Германии.
— А как попасть в эти центры пациенту из другого региона?
— Лечащий врач направляет человека к нам на консультацию. Пациенты приезжают в центр, и если, рассмотрев медицинские документы, специалисты понимают, что трансплантация необходима, человека включают в лист ожидания.
«Костный мозг — это орган, поэтому его можно взять только однократно»
— Как трансплантация от родителей к детям вообще стала возможной? Раньше были только от брата или сестры.
— Изменилась технология трансплантации, которая позволила уменьшить риск осложнений при выполнении пересадки клеток от родителей. Была проведена колоссальная работа: различные анализы, разработка протоколов, длительная подготовка, что привело к той технологии, которая сейчас сопоставима с другими методами пересадки, например, от неродственных доноров.
— Задам глупый вопрос: а почему нельзя взять клетки от бабушки и дедушки?
— Да, от бабушки или дедушки нельзя (смеется), как от жены или мужа. Потому что каждый родитель имеет набор генов от своих родителей — бабушки и дедушки, а внуки — от своих. Теоретически такая пересадка возможна, но практически очень маловероятна — у нас, по крайней мере, ни разу не было такого, а вот от тети или дяди пересадки были.
— Получается, что условный неродственный донор на другом конце мира может быть больше подходящим, чем бабушка или дедушка?
— Точно, да. Вероятность того, что внук возьмет такой же гаплотип, как его родители, очень маленький. Поэтому мы даже не анализируем это направление.
Гаплотип — совокупность аллелей на локусах одной хромосомы, обычно наследуемых вместе.
— А если на процесс типирования посмотреть именно с технической стороны, то как происходит? Берется некая проба?
— Да, речь идет о молекулярно-биологическом типировании. Есть специальное оборудование, которое позволяет провести его на высокоточном уровне. По сути, это специальная лаборатория, занимающаяся типированием.

— А поиск донора происходит автоматизированно сейчас?
— Предварительный поиск — да. Система показывает варианты, в том числе информацию о том, где живут потенциальные доноры. Безусловно, они могут быть из самых разных стран мира. Если говорить о российском регистре, то — из разных городов. Мы оцениваем, где проживает наибольшее количество потенциальных доноров. И дальше уже обращаемся в регистр, чтобы там провели подробное обследование доноров. Когда там находят совместимого человека, сообщают нам.
— А как находится эта максимальная совместимость? Есть какие-то показатели?
— Да, в специальных лабораториях последовательно проверяется совместимость донора по генам HLA-системы — системы гистосовместимости.
Человеческие лейкоцитарные антигены, или система тканевой совместимости человека (от англ. HLA, Human Leukocyte Antigens) — группа антигенов гистосовместимости, главный комплекс гистосовместимости у людей. Представлены более чем 150 антигенами.
— И какое количество этих показателей должно совпасть, чтобы этот донор был совместим?
— В идеальном варианте 10. Но можно девять, поскольку иногда сложно найти полностью совместимого человека.
— У профессора Афанасьева была идея создать регистр малых народов. Зачем это было нужно?
— Эта проблема существовала давно — для представителей малых народов было труднее находить доноров. Но сейчас мы по-другому к этому относимся, поскольку появилась возможность трансплантации от гаплоидентичного донора — от родителей. Поэтому такой зависимости от неродственных доноров нет.
Но в целом это проблема народов, которые долгое время жили на одной территории и ни с кем не смешивались. Хороший пример — Япония: живут на одном острове, практически изолированно, там мало смешанных браков с представителями других национальностей. Поэтому японцы не могут пользоваться международными регистрами, но пользуются своими, которые развиты очень хорошо.
— Почему стать донором костного мозга можно лишь один раз?
— Потому что это операция. А во-вторых, костный мозг — это орган, поэтому его можно взять только однократно.
— А это обусловлено законодательством? Чисто теоретически это можно делать несколько раз?
— Бывают ситуации, когда тому же человеку нужно выполнить повторную трансплантацию, тогда мы можем снова обратиться к донору и при условии его согласия взять клетки еще раз. А для другого пациента — это уже невозможно. С точки зрения науки, это скорее вопрос этики.
— Как изменилась терапия после ТКМ — в восстановительный период? Все ли еще высок риск возникновения реакции «трансплантат против хозяина» (РТПХ)?
— Изменились схемы лекарственных препаратов. Мы стали обращать внимание на большее количество деталей при сопроводительной терапии. Но это касается не технологии в целом, а скорее, практических вопросов.
Возникновение РТПХ зависит от многих причин, иногда вероятность возникновения такой реакции — от 40% до 50%. При лейкозах РТПХ имеет лечебный эффект, поскольку иммунный конфликт работает против заболевания и рецидивов. При незлокачественных заболеваниях, напротив, нам нужно максимально избежать такой ситуации, она мешает лечению.
Реакция «трансплантат против хозяина» — это серьезное, опасное для жизни осложнение трансплантации гемопоэтических клеток. Возникает, когда иммунные клетки донора (трансплантат) воспринимают обычные клетки тела реципиента (хозяина) как инородные и атакуют их.
— Вы сказали, что появились новые препараты для терапии во время восстановительного периода?
— Даже, скорее, не препараты, а технологии. Например, есть один препарат — циклофосфамид, который уже много лет применяется в нашей области, но мы никогда не использовали его как профилактику. Однако проведенные исследования показали, что если его ввести в терапию на определенный период после трансплантации, то вероятность развития РТПХ существенно снижается.
— Когда становится понятно, что ТКМ и лечение прошли успешно и пациент полностью выздоровел?
— Есть несколько критических периодов. 100 дней — ранний восстановительный период, затем шесть месяцев. После чего пациента наблюдают ежегодно в течение пяти лет. Встречи могут продолжаться, но это уже личное желание — все-таки это очень важная история в жизни и врача, и пациента.
«Когда понимаем, что исчерпали все варианты, переходим к подготовке к ТКМ»
— Сегодня регулярно выходят новости о применении ТКМ для лечения рассеянного склероза или ВИЧ. То есть процедура расширяет свой «функционал»?
— Да, но механизм лечебного действия при каждом заболевании имеет свои особенности. Сама технология трансплантации тоже различная: это могут быть клетки другого человека или собственные.

— Но ТКМ до сих пор остается крайней мерой лечения?
— Безусловно, это опасный метод, и, конечно, если есть возможность не трансплантировать, мы стараемся использовать все ресурсы современной медицины консервативного характера. А когда понимаем, что исчерпали все варианты, переходим к подготовке к ТКМ.
— А какие-то альтернативы ТКМ за эти 30 лет появились?
— Конечно, сейчас очень развиваются таргетные препараты — точечного воздействия, а также препараты иммунной терапии. Пока таких препаратов, излечивающих заболевание, практически нет, но за ними, безусловно, будущее. Правда, уже появился один, при хроническом миелолейкозе — ингибитор тирозинкиназ.
Не исключено, что в некоторых ситуациях, эти лекарственные препараты будут иметь преимущество по сравнению с трансплантацией. Пока это вопрос времени.
СПРАВКА
Благотворительный фонд AdVita с 2002 года помогает взрослым и детям, которые лечатся от рака в клиниках Петербурга, и онкологическим отделениям больниц.
Задача фонда — сделать современное лечение доступным любому человеку независимо от возраста, уровня дохода, медицинского прогноза. Мы помогаем на всех этапах: от постановки диагноза до завершения лечения. AdVita оплачивает диагностику, лекарства, поиск донора костного мозга, оборудование для клиник и расходные материалы к нему.
В 2020 году адресную помощь фонда получили 740 человек из 75 регионов Российской Федерации. Системную поддержку получили пациенты четырех онкологических клиник Санкт-Петербурга, две из которых — федеральные, в них проходят лечение люди со всех регионов страны.
Читать далее
Зонд Mars Express «пообщался» с китайским ровером на Красной планете
Исследование из Китая: штамм омикрон обходит защиту от вакцинации и перенесенного COVID-19
Посмотрите на рыбу с прозрачным лбом: ее мозг и глаза видно сквозь голову
