В недавно опубликованном исследовании в журнале Cell Genomics сотрудники Бернского университета и больницы Инсел нашли новые «мишени» для лечения рака — в «темной материи» генома. «Хайтек» рассказывает, что это такое.
Рак — вторая по значимости причина смерти в Швейцарии. Среди различных видов рака, один из самых опасных — немелкоклеточный рак легкого (НМРЛ). Он убивает большинство пациентов и, в основном, остается неизлечимым. К сожалению, даже недавно одобренные методы лечения могут продлить жизнь пациентов всего на несколько месяцев. Лишь немногие выживают в долгосрочной перспективе на стадии появления метастаз. Поэтому ученые активно ищут новые методы лечения.
«Темная материя» генома — что это?
В качестве новых мишеней они использовали малоизученный класс генов — длинную некодирующую РНК (рибонуклеиновыми кислотами) или днРНК.
днРНК (англ. long non-coding RNAs, lncRNA) — некодирующие РНК, чья длина, как правило, составляет более 200 нуклеотидов, и расположены в ядре или в цитоплазме. Точное количество lncRNAs в клетках человека неизвестно до сих пор. Считается, что в геноме человека присутствуют около 15 000 днРНК.
Длинные некодирующие РНК существуют в изобилии в так называемой «темной материи» генома. Той части ДНК, которая не кодирует белок и составляет его подавляющее большинство. Геном содержит около 20 000 «классических» генов, кодирующих белки. Но это число ничтожно мало на фоне 100 000 днРНК. Биологические функции 99% днРНК неизвестны.

Как следует из их названия «длинные некодирующие РНК», в отличие от матричных РНК (мРНК), днРНК не кодируют планы построения белков. Как и в случае с мРНК, инструкции по построению днРНК содержатся в клеточной ДНК.
Подготовка к эксперименту
Чтобы изучить роль днРНК в НМРЛ, исследователи изучили общедоступные наборы данных. В результате ученые составили более чем 800 днРНК, важность которых для клеток рака биологи и хотели проверить. Для этого они разработали специальную систему скрининга, которая предотвращает производство выбранных днРНК путем удаления части инструкций по их строению в самой ДНК.
Ученые уже применили систему скрининга к двум клеточным линиям НМРЛ, полученным от пациентов. А затем — посмотрели, как ингибирование выбранных днРНК влияет на отличительные признаки раковых клеток. Они включают поведение, которое способствует прогрессированию заболевания: пролиферация, образование метастазов и резистентность к терапии.
В итоге, из 800 исследованных кандидатов биологи составили список из всего 80 днРНК с высокой степенью достоверности, которые важны для НМРЛ. Далее, из этих 80 ученые выбрали всего несколько для последующих экспериментов.
Как проходило исследование?
Для последующих экспериментов биологи использовали подход, который не работает на уровне ДНК, а нацелен именно на днРНК после их образования. С этой целью ученые использовали малые химически синтезированные РНК — антисмысловые олигонуклеотиды (АСО). Они связываются с днРНК, на которые нацелены, и приводят к их деградации. Следует отметить, что несколько АСО уже одобрены для лечения заболеваний человека, но пока ни одного для лечения рака.
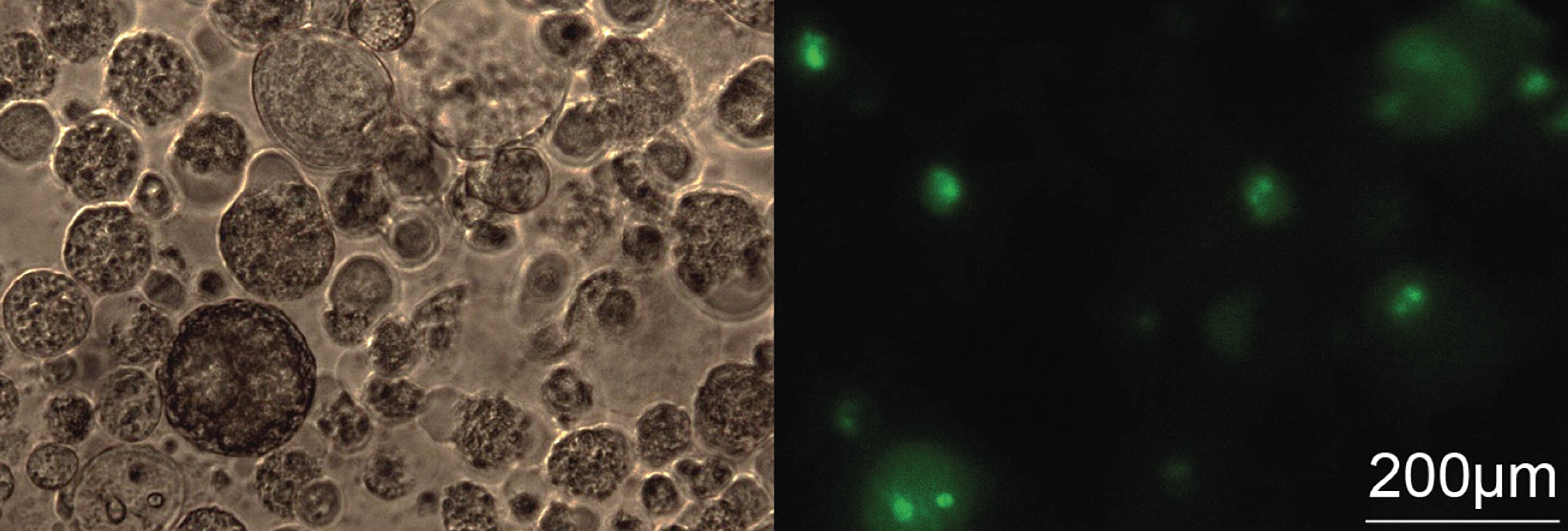
Предоставлено: UniBE/NCCR
Антисмысловые олигонуклеотиды — это одноцепочечные химически модифицированные фрагменты ДНК, «целью» которых служат пре-мРНК, короткие фрагменты генетической информации, которые потом выступают в качестве «инструкции» для рибосомы, собирающей по ним белки. В зависимости от того, как работает конкретный антисмысловой олигонуклеотид, мРНК в итоге либо разрушается, либо иначе проходит сплайсинг — процесс, в котором те или иные экзоны (кодирующие участки) либо включаются в итоговую мРНК, либо исключаются из нее.
Что показал эксперимент?
Последующие эксперименты показали, что для большинства отобранных днРНК их разрушение с помощью АСО ингибирует деление раковых клеток в клеточной культуре. Важно отметить, что такое же лечение практически не повлияло на незлокачественные клетки легких, которым не должно быть нанесено вреда при лечении рака. В 3D-модели НМРЛ, которая больше напоминала опухоль, чем клеточную культуру, ингибирование одной днРНК с помощью АСО уменьшало рост опухоли более чем наполовину.

Как отмечают авторы исследования, они были «приятно удивлены, увидев, насколько хорошо антисмысловые олигонуклеотиды сдерживают рост опухоли в различных моделях».
Что дальше?
Исследователи продолжают исследования доклинических моделей рака и рассматривают возможность сотрудничества с существующими компаниями или создания стартапа для разработки препарата для лечения пациентов.
Что касается других видов рака, ученые заявили — их подход должен легко адаптироваться для выявления новых потенциальных методов лечения для других типов рака. Следующая цель — колоректальный рак. Он — третий по частоте появления злокачественных новообразований в мире Ежегодно во всем мире от колоректального рака умирает около 880 000 человек. Во всем мире ежегодно диагностируют около 1,8 млн новых случаев этого заболевания. Это — важная цель.
Читать далее:
Неизвестный вид крылатых насекомых «скрывался» в янтаре более 35 млн лет

